금
다른 표기 언어 Gold , 金| 분류 | 전이 금속 |
|---|---|
| 원자번호 | 79 |
| 원소기호 | Au |
| 상태 | 고체 |
| 원자량 | 197 |
| 녹는점 | 1,063℃ |
| 끓는점 | 2,966℃ |
| 원자가 | 1, 3 |
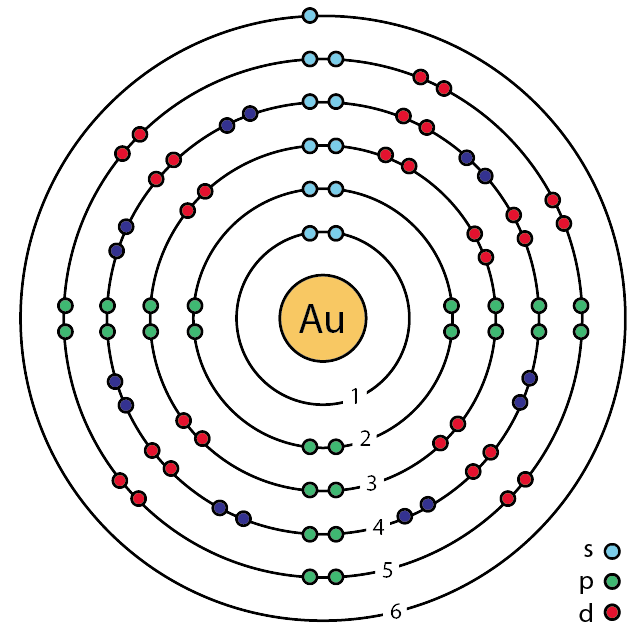
| 전자배열 | 2-8-18-32-18-1 또는 (Xe)4f145d106s1 |
| 비중 | 19.3(20℃) |

조밀하고 귀중한 밝은 황색의 광택이 있다. 금은 좋은 열·전기 전도체로 연하며, 금속 중에서 전성과 연성이 가장 좋다. 28g의 금을 두드려 30㎡까지 펼 수 있으며, 얇은 금박(leaf)은 녹색광선을 투과시킨다. 이 희유금속은 천연에서 비교적 순수한 형태로 존재하며, 시각적으로 아름답고, 가공하기 쉽고, 변색되거나 부식되지 않기 때문에 인간의 관심을 끈 최초의 금속 가운데 하나가 되었다.

이집트·크레타·아시리아·에트루리아의 장인들은 금으로 아름답고 정교한 예술품을 제작했으며, 금을 상품이나 용역을 교환하는 수단의 하나로 쓰기도 했다(→ 장신구, 금세공품). 다른 여러 금속들과 마찬가지로 금은 화강암에 소량으로 널리 퍼져 있다. 지각에서 산출되는 금은 대략 0.005ppm 정도로 추산된다. 금은 대체로 천연상태로 산출되며, 텔루륨이나 아마도 셀레늄과 비스무트 화합물을 제외하고는 화학결합을 하지 않는다.
천연 금의 동위원소는 모두 197Au이다. 광석이라 할 만큼 다량의 금을 함유한 암석은 드물다. 상당량의 금을 함유한 광상은 2종류로, 석영과 황철석(바보금)이 섞여 있는 열수광맥과 금을 함유한 암석의 풍화에 의해 형성된 고화 혹은 비고화 사광광상이 있다(→ 사력광상, 열수광상).
금을 많이 함유하는 광맥은 기원이 정확히 알려져 있지는 않으나, 심부의 금이 최소한 부분적으로 다른 광물들과 함께 적어도 부분고용체로 위로 운반되다가 침전하는 것으로 추측된다. 금은 암석에 대개 눈에 띄지 않는 작은 입자로 산재하여 있다. 그러나 눈에 보일 정도 크기의 엷은 층으로 되어 있는 경우도 간혹 있으며 덩어리로 또는 세맥으로 되어 있는 경우도 아주 간혹 있다. 지름이 약 2.5㎝ 이상되는 결정이 미국 캘리포니아에서 발견된 적이 있으며, 90㎏이나 나가는 덩어리가 오스트레일리아에서 나오기도 했다.
지금까지 채굴된 모든 금의 약 60%는 각국의 정부와 중앙은행이 보유하고 있다(→ 화폐). 이는 각국 지폐 현금을 밑받침해줄 뿐만 아니라, 이제까지 가장 중요한 국가간 지불수단으로 사용되어왔다. 예술재료로서의 가치도 계속 유지되고 있다. 보석에 쓰이는 금은 보통 은·팔라듐·백금과 합금된다. 합금 속에 포함된 금 함량은 캐럿이라는 24단계로 표시된다. 12캐럿 금 합금은 50%의 금을 포함하고, 24캐럿 금은 순수한 금이다.
금은 비활성과 높은 전기전도도(구리의 71%)를 갖고 있기 때문에, 대부분 공업적으로 도금단자·인쇄회로·반도체 등과 같은 전기·전자 공업에 광범위하게 사용된다. 얇은 금 필름은 입사된 적외선의 98%까지 반사시키기 때문에 인공위성의 온도조절용 피막으로 우주복 방호를 위해 사용되고 있다. 이와 유사한 용도로, 사무용 대형건물의 창에 사용되어 에어컨의 사용을 줄이고 미관을 더해주기도 한다. 또한 치아의 충전물 및 기타 보조재료로 오랫동안 사용되어 왔다. 루비 유리의 화려한 붉은 색깔은 콜로이드상으로 분산된 미량의 금에 의한 것이다.

| 국가 | 1991년 채광량 (t) |
전세계 채광량 (%) |
1991년 확인된 매장량(t) |
전세계 확인된 매장량(%) |
| 남·북아메리카 | ||||
| 미국 | 300 | 14.6 | 5,250 | 10.6 |
| 브라질 | 70 | 3.4 | 1,080 | 2.2 |
| 캐나다 | 170 | 8.3 | 1,960 | 4.0 |
| 아시아 | ||||
| 중국 | 110 | 5.3 | ... | ... |
| 아프리카 | ||||
| 남아프리카 공화국 | 600 | 29.1 | 22,000 | 44.5 |
| 오세아니아 | ||||
| 오스트레일리아 | 230 | 11.2 | 2,700 | 5.5 |
| 기타 | 580 | 28.2 | 16,490 | 33.3 |
| 세계 합계 | 2,060 | 100.0 | 49,480 | 100.0 |
| 자료 : 미국 상무부, 〈광물 상품 요략〉, 1992 | ||||
금 화합물
금의 주요 산화수는 +1가와 +3가이다. 금은 전기화학 계열의 가장 밑바닥에 위치하는데, 심지어 백금이 Au3+를 환원시켜 금속상태의 금으로 환원시킨다.
실제로 덜 중요한 금 화합물로는 염화금(Ⅰ)(AuCl)과 염화금(Ⅲ)(AuCl3), 클로로금(Ⅲ)산(HAuCl4)이 있다.
이 3가지 화합물은 모두 금의 전기정련에 사용된다. 시안화금(Ⅰ)산칼륨(K[Au(CN)2])은 대부분 금 도금액(금을 도금할 때 사용하는 용액)의 주성분이 된다. 수용성 사클로로금(Ⅲ)산나트륨(NaAuCl4·2H2O)은 류머티즘 치료에 쓰인다. 금의 몇몇 유기화합물들은 공업적으로 사용되기도 한다. 예컨대 황화테르펜에서 얻은 금머캅타이드는 특정 유기용액에 용해되어 접시나 유리제품의 장식제로 사용된다.