수산화물
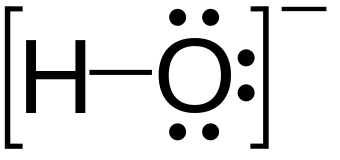
다른 표기 언어 hydroxide , 水酸化物요약 어떤 원소가 음전하를 띤 수산화 이온(OH-, 1개의 산소원자와 수소원자가 서로 결합하여 만든 이온)을 하나 이상 포함하는 화합물.
화합물 내의 양이온은 보통 금속 이온(예를 들어 나트륨·마그네슘·알루미늄 등)이며, 구아니딘이나 테트라메틸암모늄 같은 유기원자단도 있다.
이온화되지 않고 공유결합으로 결합된 히드록시기(OH)는 히드록시아세트산(CH2OHCOOH)에서처럼 히드록시(hydroxy)라는 접두어를 써서 나타낼 수도 있고, 메탄올(CH3OH)에서처럼 올(ol)이라는 접미사를 써서 나타낼 수도 있다. 테트라히드록소금(Ⅲ)산칼륨(KAu(OH) 4)과 같은 배위결합 화합물에서는 히드록소(hydroxo)라는 접두어를 쓴다.
실험실과 공장에서 많이 쓰는 수산화물에는 여러 종류의 염이 있다. 알칼리 금속인 리튬·나트륨·칼륨·루비듐·세슘의 수산화물은 강염기로 가장 안정하며, 수산화물 가운데 가장 잘 용해된다. 가성소다 혹은 잿물로 잘 알려져 있는 수산화나트륨(NaOH)은 공업적으로 매우 중요한 물질이다. 칼슘·바륨·스트론튬과 같은 알칼리 토금속은 가용성 수산화물을 만들며, 강염기이지만 알칼리 금속의 수산화물보다는 덜 안정하다. 이들 중에서는 소석회라고도 하는 수산화칼슘(Ca(OH) 2)이 가장 잘 알려져 있다.
수산화탈륨(TlOH)을 제외하고는 마그네슘·철·비스무트·니켈·코발트·구리와 같은 금속의 수산화물은 물에 거의 녹지 않으나 산을 중화시킨다. 베릴륨·납·아연·알루미늄·크롬(Ⅲ)·주석(Ⅱ)·금(Ⅲ)과 다른 몇몇 금속의 수산화물은 산과 염기의 특성을 모두 갖고 있다. 즉 이들은 염기성 수용액과 산성 수용액에 모두 용해된다. 이와 같이 산과 염기의 2가지 성질을 모두 가지고 있는 수산화물·산화물·황화물 등을 양쪽성 화합물이라고 한다.